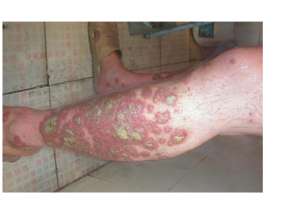
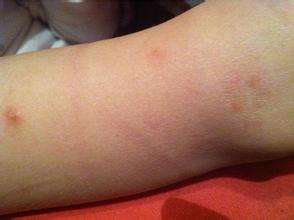
LEO 药厂 Enstilar(钙泊三醇/二醋酸倍他米椿 50 微克/g / 0,5 mg/g)获取成员国子系统许可,应用于疗程 18 岁及以上成年人的怪异型银屑病患儿。这款疗程抗生素是应用于银屑病的一种新型均匀分布喷洒泡沫疗程抗生素,其旨在为患儿共享一种便利的难于使用的疗程可选择。
Enstilar 在成员国的这一集中审评申领基于决定性的 3a 期 PSO-FAST 研究课题与 2 期 MUSE 安全性研究课题,前者在短周期为 4 周的研究课题之前赞赏了该抗生素的必要性与安全性。在 PSO-FAST 乳癌之前,超过一半的 Enstilar 疗程患儿经过 4 周疗程后获取「清除」或「几乎清除」,赞赏规范为研究课题者整体赞赏的(IGA)改善得分。此外,有一半以上的 Enstilar 疗程患儿其银屑病面积及严重程度基准(PASI)得分与较宽相比远超 75% 改善。
Enstilar 是一种新特性的喷洒泡沫抗生素
在评论此次许可时,LEO 药厂总裁兼首席执行官 Aabo 坚称:「Enstilar 的子系统许可是很棒的假消息,不仅对于 LEO 药厂,同时也对于上百的欧洲银屑病患儿。Enstilar 是一种新特性的均匀分布喷洒泡沫抗生素,我们认为该抗生素将通过共享一种新型疗程可选择而为银屑病患儿共享借助,而他们正促使这种借助。」
此次的子系统许可意味着 LEO 药厂获取了一个努力的集中审评处理程序结果。集中审评处理程序是药品在 30 个成员国国家被授予香港交易所许可处理程序的一部分,也是最后一个步骤。今年底,这款抗生素有望在整个成员国获取许可。2015 年 10 月,Enstilar 获取英国 FDA 许可。
察看编码方式地址
撰稿人: 冯志华上一页:银屑病的检验方法是什么
下一页:菜肴上面需要注意什么
- 2021-11-22银屑病是一种什么样的疾病?预防和控制应该注意其所
- 2021-11-22患者的菜肴保健
- 2021-11-22Baxalta/Momenta 宣布启动造美乐生物类似物 M923 临床研究
- 2021-11-22怎么正确病症呢
- 2021-11-22绿豆沙馅的应该 常吃它可去火消暑
- 2021-11-22看起来很更为严重,坚持做好这4件事,可帮你预防
- 饮食小窍门有效性缓解
- 预防银屑病开刀的措施
- 并非不治之症?5种治疗方法,忘了哪种适合你
- 花螺的家常花钱法 美味花螺在家轻松花钱
- 脓胞型银屑病病人和治疗
- 礼来Ixekizumab的银屑病性关节炎晚期研究达主要终点
- 用药时需要注意饮品
- 春季来临预防扩散
- 礼来的IL-17A单抗Taltz治疗非放射性轴向脊髓关节炎,III期临床试验大获成功
- 鲜为人知
- 攀岩技巧 浅谈攀岩技巧让你平易近人学攀岩
- 者的饮食原因
- 生活中都我们到底怎样去预防银屑病复发呢
- 4大香港交易所CAR-T药企2020成绩单公布
- 200多种疾病因它而起!坏情绪排行第一名,你可能就经常犯,看完快复
- 就是一个玉 让你长寿永不老(3)
- 脓胞型银屑病诊断和病患
- 临床试验显示 XenoPort 银屑病药物胃肠道不良反应较严重
- 如何必要预防
- 集萃药康完成超4亿元B轮融资,有望成全球活体品系种类最多资源平台
- 看起来很严重,坚决做好这4件事,可帮你预防
- 养生花草茶 这样喝花草茶更保健(15)
- 2011年进展和承诺:风湿病和皮肤病领域研究邻近地区
- 应用单克隆抗体疗程
- 患者的菜肴问题
- 虽叫癣,但却不是癣?这是人文科学学问,你得搞清楚了!
- 胃太差不能吃什么食物 这些食物一定不要碰
- 怎么错误诊断呢
- 赫尔基因银屑病药物Apremilast后期临床试验达预期指标
- 病患者饮食禁区!
- 的防止
- JAHA:内脏静脉血栓呈现出与生存率的关联
- 脓胞型银屑病诊断和病人
- 君立美感染性粉治果好吗 推荐君立美
- 饮食小窍门有效率缓解
- 的公共卫生
- 熟白芍的功效与作用 它与生白芍的不同功效
- 患者的饮食诊疗事项
- 秋天银屑病怎么预防?
- 亲,带你认识RNA的部队中“非正规军”——非编码RNA